국내개발 백신 ‘제넥신 GX-19’ 초기단계 임상시험 중
혈장치료제 임상 신청 예정
[이코노미21 임호균 기자] 신종 코로나바이러스 감염증(코로나19) 확산세가 지속되면서 치료제와 백신의 개발 상황이 어떻게 진행되고 있는지 관심을 모으고 있다. 식품의약품안전처는 현재 우리나라에서 코로나19 관련 진행 중인 임상시험은 치료제 10건, 백신 2건 등 총 12건이라고 10일 밝혔다.
현재 임상시험을 승인받은 기업 및 연구기관은 ∆강남세브란스병원 ∆고대 구로병원 ∆경상대병원 ∆국제백신연구소 ∆길리어드사이언스코리아 ∆동아대병원 ∆대웅제약 ∆부광약품 ∆서울대병원 ∆서울아산병원 ∆신풍제약 ∆엔지컴생명과학 ∆종근당 ∆제넥신 ∆크리스탈지노믹스(가나다 순) 등이다.
크리스탈지노믹스의 CG-CAM20와 대웅제약의 DWJ1248 2건은 지난달 26일 발표 이후 임상시험이 추가 승인됐다. 두 제품은 이미 허가된 카모스타트 성분 의약품을 이용해 개발 중이며 이 성분은 만성 췌장염 및 역류성 식도염 치료제로 사용되고 있다. 특히 카모스타트 성분은 세포 단계의 초기 시험에서 코로나19 바이러스 활성화를 억제하는 것으로 확인됐다. 미국, 영국, 독일 등 5개국에서도 이 성분을 이용한 임상시험이 진행 중이다.
한편 렘데시비르 3건과 옥시크로린정-칼레트라정 1건, 할록신정 1건은 임상시험이 종료됐다. 렘데시비르는 계획대로 임상시험이 완료돼 현재 특례수입으로 환자들에게 공급하고 있다. 옥시크로린(성분명 히드록시클로르퀸)·칼레트라(로피나비르·리토나비르) 비교 임상과 할록신정(히드록시클로르퀸) 임상은 주요 성분인 히드록시클로르퀸이 코로나19 치료에 유익성이 인정되지 않는다는 해외 연구결과에 따라 종료됐다.
현재 진행 중인 백신은 2건으로 모두 초기단계인 임상1상~2상에 있다. 국내 개발 백신으로는 제넥신의 GX-19로 초기단계 임상시험 중이다.
임상시험 계획을 심사 중인 코로나19 치료제와 백신은 5건이 있다. 심사 중인 5개 제품은 모두 국내 개발 치료제다. 국내에서 코로나19 환자에게 투입해 효과가 있는 것으로 관심을 끌었던 혈장치료제도 조만간 임상 신청을 할 것으로 알려졌다. 이밖에도 상담이 이뤄지고 있는 의약품은 33개에 달한다.
현재 심사 중인 5개 제품은 신약 항체 치료제 1개, 약물 재창출 치료제 4개 등으로 모두 국내 개발 치료제다.
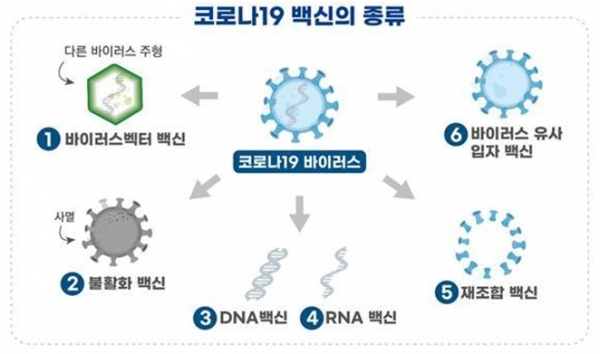
현재 전 세계에서 개발되고 있는 코로나19 백신 종류로 바이러스벡터 백신, 불활화 백신, DNA 백신, RNA 백신, 재조합 백신, 바이러스 유사입자 백신 등이 있다.
코로나19가 장기화, 재확산하면서 치료제와 백신 개발을 위한 각국의 경쟁은 더욱 치열해지고 있다. 미국과 중국이 가장 적극적으로 개발에 나섰으며 우리나라도 정부의 지원 아래 치료제와 백신 개발에 공을 들이고 있다. 우리나라가 세계 최초로 코로나19 진단키트를 개발한 것처럼 치료제와 백신개발에도 다른 나라보다 먼저 성과를 낼지 주목된다. [이코노미21]